Nature Cancer:儿童脑瘤疫苗新进展:靶向巨细胞病毒的I期临床试验
15小时前 儿童肿瘤前沿 儿童肿瘤前沿 发表于上海
研究证实,PEP-CMV 在该人群中安全可耐受,并能显著诱导抗原特异性 T 细胞免疫应答,为探索基于病毒抗原的脑肿瘤免疫治疗策略奠定了临床与机制双重基础。
过去几十年间,儿童脑瘤的总体预后已显著改善,约55%-80%的患儿经治疗后可存活五年以上,但这仅为平均数据。部分类型的肿瘤,如高级别胶质瘤( HGG),其预后仍然较差。数据显示,复发性胶质母细胞瘤患儿的中位生存期约为一年;而高级别胶质瘤患儿的中位生存期则约为16个月。这类肿瘤发病机制复杂、治疗困难,严重威胁患者生命。
近日,杜克大学神经肿瘤免疫团队在 Nature Cancer 上发表了一项题为 A peptide vaccine targeting the CMV antigen pp65 in children and young adults with recurrent high-grade glioma and medulloblastoma: a phase 1 trial 的研究。该团队通过一项单臂 I 期临床试验,评估了靶向巨细胞病毒(CMV)pp65 抗原的多肽疫苗(PEP-CMV)在复发性高级别胶质瘤及髓母细胞瘤儿童和青年患者中的安全性。研究证实,PEP-CMV 在该人群中安全可耐受,并能显著诱导抗原特异性 T 细胞免疫应答,为探索基于病毒抗原的脑肿瘤免疫治疗策略奠定了临床与机制双重基础。

在详细解读该临床试验结果前,先简要介绍巨细胞病毒(CMV)与儿童脑瘤的关联,以及新型免疫疗法——多肽疫苗的相关背景知识。
巨细胞病毒与儿童脑瘤
巨细胞病毒(Cytomegalovirus, CMV)属于疱疹病毒家族,是一种广泛存在的病毒。多数人在幼年时期即已感染 CMV,此后病毒长期潜伏于体内,被免疫系统抑制而处于休眠状态。据统计,约 50%~80% 的成年人在 40 岁左右时血清中可检测到既往 CMV 感染的迹象。对于免疫功能正常者,CMV 通常不引起明显疾病,仅在免疫力低下(如艾滋病患者、器官移植受者)或胎儿期感染时可能造成严重后果。
CMV 并非公认的直接致癌病毒,因其本身不携带明确的致癌基因,也并非必然导致细胞癌变。然而,自 2002 年首次报道以来,多项研究在多种恶性脑肿瘤组织(如高级别胶质瘤和髓母细胞瘤)中检测到了 CMV 的存在。例如,研究发现 CMV 的 pp65 抗原在肿瘤组织中有表达,但在邻近的正常脑组织中却检测不到。这表明这些肿瘤细胞中存在 CMV 成分。
鉴于 CMV 成分特异性存在于肿瘤组织中,其抗原(如 pp65)便成为潜在的理想免疫靶点。科学家设想,通过疫苗策略诱导免疫系统识别 CMV 抗原,可能实现“一箭双雕”的效果:既清除肿瘤内潜伏的病毒,又杀伤表达病毒抗原的肿瘤细胞。因此,以 CMV 抗原(如 pp65)为靶点的多肽疫苗(如 PEP-CMV)应运而生,旨在利用病毒抗原激发抗肿瘤免疫应答。
多肽疫苗的原理与肿瘤免疫治疗
多肽疫苗通过将特定肿瘤抗原的短肽片段(通常为 8-12 个氨基酸)合成后,与佐剂一同注射入体内。这些肽段可被抗原呈递细胞(如树突状细胞)摄取、加工,并装载到其表面的主要组织相容性复合体(MHC)分子上,进而呈递给 T 淋巴细胞。此过程旨在训练免疫系统识别并清除表达相应抗原的癌细胞。
多肽疫苗通常选取肿瘤相关抗原(TAA)或肿瘤特异性抗原(TSA)的免疫原性肽段。通过 MHC 分子的“展示”,可激活细胞毒性 T 细胞(CTL),使其能够特异性识别并杀伤表面呈现相应抗原肽-MHC 复合物的肿瘤细胞。
简而言之,多肽疫苗如同为免疫系统提供一张“通缉令”(即肿瘤特异性蛋白片段),使其能够识别目标,进而在体内搜寻并清除携带该片段的肿瘤细胞。


PEP-CMV 的安全性
PEP-CMV I期临床试验的主要终点为安全性,研究团队将不可接受毒性(unacceptable toxicity)的发生率作为核心评价指标。该试验共入组了40例复发性高级别胶质瘤(HGG)患者。
所有观察到的疫苗相关不良事件(adverse event, AE)中,绝大多数为低级别(1-2级)事件:包括17例1级AE和15例2级AE。仅报告了1例被认为与疫苗相关的3级AE(锥体束征)和1例4级AE(脑水肿)。
不可接受毒性事件的发生率低于方案预设的阈值,表明PEP-CMV在该患者人群中总体耐受性良好,安全性良好。主要安全性终点达成。
免疫应答结果
T细胞免疫应答: 在21位能评估免疫反应的患者中,疫苗成功激起了针对CMV pp65抗原的T细胞反应。接种后,血液检测(IFN-γ ELISpot)显示针对pp65的反应强度平均提升了约46个斑点(范围在8到194个之间)。这意味着大多数患者体内都产生了能识别pp65的“杀手”T细胞(CD8⁺)和“指挥官”T细胞(CD4⁺)。更有意思的是,随着接种次数增加,这些T细胞变得更“能干”——能同时释放多种“战斗信号”(如IFN-γ、TNF-α、IL-2)的T细胞比例显著上升了。
NK细胞变化: 疫苗还影响了另一种重要的免疫士兵——自然杀伤细胞(NK细胞)的队伍构成。接种后,血液中一种具有“调节”潜能的特殊类型NK细胞(CD56bright CD16dim)的比例增加了。这可能反映了疫苗对先天免疫系统的调动作用。不过,这种NK细胞的变化对治疗效果的影响尚不清楚。
疗效指标(病情控制和生存时间)
研究也初步观察了疫苗对控制病情和延长生命的效果(作为探索目标)。入组患者主要是多次复发、病情很重的高级别胶质瘤患者,他们的疾病进展很快:平均仅2.5个月(95% CI:2.2~3.2)后肿瘤就再次生长;平均总生存期为6.5个月(95% CI:4.6~8.4)。
尽管整体生存期较短,但在如此难治的患者群体中,仍有约27%的患者生存时间达到了1年或以上。这个结果被认为对于经历过多轮治疗仍复发的患者来说,是一个值得关注的积极苗头。
补充说明: 试验中也入组了2位复发的髓母细胞瘤患者,但他们的病情在2个月内迅速恶化或去世,未能来得及进行免疫效果的评估。
特定亚组分析
CMV感染史(血清状态):
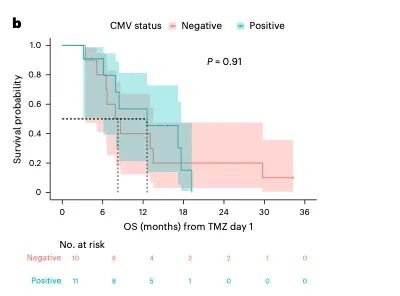
有CMV感染史(血清阳性)的患者,接种疫苗后产生的免疫反应更强。因为他们体内原本就存在针对pp65的记忆T细胞,相当于有“预备队”。
没有CMV感染史(血清阴性)的患者,接种后也能产生针对pp65的新T细胞反应,只是强度相对弱一些。
在携带特定基因(HLA-A2)的患者中,有CMV感染史的似乎有病情稳定期(PFS)和总生存期(OS)延长的趋势,但患者数量太少,无法得出确定结论。
HLA-A2基因型:
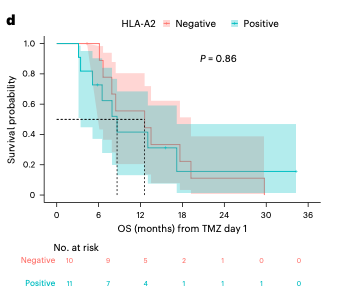
疫苗设计的靶点正好能被HLA-A2基因型的免疫系统更有效地识别。因此,携带HLA-A2基因的患者更容易产生强烈的、由CD8⁺ T细胞主导的反应;而不携带的患者则主要依赖CD4⁺ T细胞的反应。
目前来看,是否携带HLA-A2基因对生存时间(PFS或OS)没有明显影响。
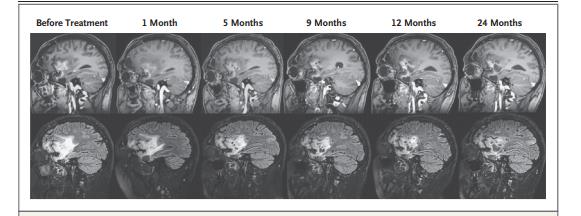
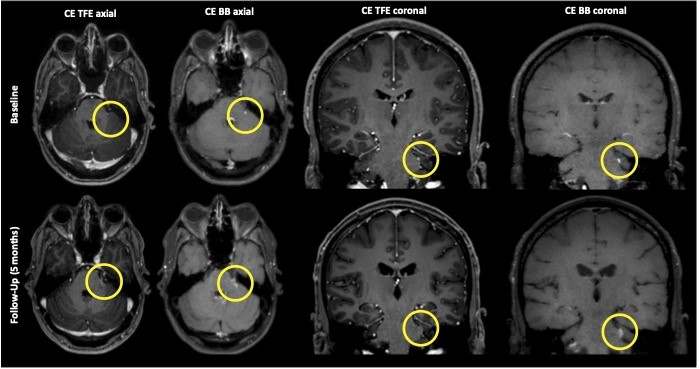
影像学评估(肿瘤大小的变化)
根据专门的脑瘤免疫治疗评估标准(iRANO)看片子,绝大多数患者在治疗后都出现了肿瘤进展(PD)。第一次复查时,很多患者肿瘤已经长大。只有极少数患者肿瘤暂时稳定(SD)了一小段时间,但很快也进展了。没有观察到肿瘤明显缩小(PR或CR)的情况。
这表明,对于这些复发的胶质瘤/髓母细胞瘤患者,PEP-CMV疫苗的主要作用可能体现在控制病情、延缓恶化,而非直接让肿瘤显著缩小——这也符合很多免疫疗法的特点。
调节性T细胞 (Treg):
打疫苗期间,患者血液中抑制免疫反应的Treg细胞比例没有明显变化。从打针前到打完第4针,Treg的数量变化非常小,没有统计意义。但是,打针前血液里Treg比例高的患者,病情进展更快,恶化风险更高(风险比约1.79)。这说明患者自身免疫系统被抑制的程度,可能影响疫苗的效果。
初始CD8⁺ T细胞:
血液中“新手”状态(Naive)的CD8⁺ T细胞数量多的患者,如果能完成多次疫苗接种,他们的病情稳定期(PFS)显著更长。这提示患者免疫系统的“后备力量”越充足,可能从疫苗中获益越多。
T细胞功能质量:
深入分析发现,疫苗确实能提升T细胞的“战斗力”。随着接种次数增加,能同时释放多种“武器”(细胞因子IFN-γ, TNF-α, IL-2)的T细胞比例越来越高,即T细胞的“多功能性”增强了。这表明持续接种有助于训练出更强大的T细胞军队。
总之,这项 I 期试验首次在复发性高级别胶质瘤(HGG)和髓母细胞瘤的儿童和青年患者中评估了 CMV pp65 多肽疫苗(PEP-CMV)。研究证实,PEP-CMV 整体安全性良好,仅报告了零星与治疗相关的 3-4 级不良事件,且未超过预设的不可接受毒性阈值;在大多数可评估患者中,疫苗成功诱导了针对 pp65 抗原的特异性 T 细胞免疫应答,并伴随T 细胞多功能性的提升,表明免疫系统被有效激活。尽管患者群体的中位无进展生存期(PFS)和总生存期(OS)仍较短,但观察到约 27% 的患者生存期达到或超过一年,为这类传统上对免疫疗法反应不佳(“免疫冷”)的脑肿瘤带来了新的希望。
综上所述,PEP-CMV 研究为利用病毒相关抗原靶向治疗脑肿瘤提供了临床可行性和免疫学机制基础,并为后续扩大样本量、探索联合免疫调节策略的研究奠定了基础。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#高级别胶质瘤# #多肽疫苗#
5 举报