抗体药物的发展历程
2025-07-07 小药说药 小药说药 发表于上海
抗体药物历经漫长发展,从免疫实践起源到理论构建,再到治疗性抗体的三代演进及多种筛选技术的应用,目前已成为生物医药重要组成,未来市场前景广阔。
-01-
引言
抗体药物是生物技术制药领域的一个重要方面。抗体具有识别抗原的特异性,因而利用抗体诊断与治疗疾病是医药研究者长期以来追求的目标。抗体与靶抗原结合具有高特异性、有效性和安全性,临床用于恶性肿瘤、自身免疫病等各种重大疾病。抗体药物的发展并不是一蹴而就的,抗体的发现以及抗体药物的临床应用经历了一段漫长的历史进程。
-02-
一、免疫实践的起源
抗体治疗的最早应用可以追溯到中国人接种“人痘”预防天花的记载算起,国际上一般公认的人痘接种术最早起源于中国公元10世纪,但据中国的一些史书记载,种痘始于唐朝。只不过当时种痘只是在民间秘密流传,没有公布于世。
随后,中国人痘接种法传入日本、俄罗斯、土耳其,并经由土耳其进一步传入欧洲。在康熙执政后,随着因得过天花而继承皇位的他开始推广人痘接种,这一技术逐渐从民间走向皇宫,得到了全国的提倡与推广。这种技术的传播对世界范围内的天花防治产生了重要影响。
到后来的英国人爱德华·琴纳受到中国人痘接种法的启示,接种牛痘预防天花,琴纳的牛痘接种法因其安全性逐步取代人痘接种,成为现代医学的重要里程碑。
-03-
二、抗体科学概念的萌芽
早在19世纪末,抗体被动免疫疗法的创立为当时不发达的疾病治疗开辟了新途径。Ehrlich提出的侧链学说为免疫学与免疫疗法奠定了基础。他认为,细胞的表面具有特异性受体分子(或称侧链),这些侧链仅与毒素分子中特定的基团结合;如果细胞与毒素结合后能存活下来,将会产生过量的侧链,部分的侧链释放至血液中,即为抗毒素,这就是现在所称的抗体。
1890年,德国生理学家 Emil von Behring 与日本微生物学家 Shibasaburo Kitasato 在研究中发现,暴露于白喉或破伤风毒素的动物血清中存在一种能中和毒素的物质(即抗体前身),将其命名为 “抗毒素”(antitoxin)。他们通过将免疫动物的血清输注给患病动物,成功治愈感染,首次证明了血清中活性物质的保护作用 。

Emil von Behring 与 Shibasaburo
1891年10月,Ehrlich在论文《免疫力的试验性研究》中首次使用德语词 “Antikörper”(抗体),并提出化学结构理论:抗体与抗原的结合遵循 “锁钥模型”(类似酶与底物),强调结构互补性是特异性结合的关键 。

Ehrlich
到现在,科学家们对于抗体有了一个公认的定义。抗体是一种由B细胞识别抗原后活化、增殖分化为浆细胞,并由浆细胞合成与分泌的、具有特殊氨基酸序列的,能够与相应的抗原发生特异性结合的免疫球蛋白分子。
-04-
三、抗体理论构建阶段
在抗体发现早期,这种特异性的抗体物质勾起了科学家们极大的兴趣,科学家们前赴后继致力于解析抗体的结构,但由于落后的实验条件,进展缓慢。直到20世纪5O年代,科学家们对抗体的结构和抗原抗体识别机理的理解还非常浅显。
1937年瑞典物理学家Arne Wilhelm Kaurin Tiselius通过电泳技术证明了抗体也是一种蛋白质,并将其称为γ球蛋白。1953年英国生物化学家Frederick Sanger成功解析了同样身为蛋白质的胰岛素的化学结构,从而为科学家们解析抗体结构指明了方向。
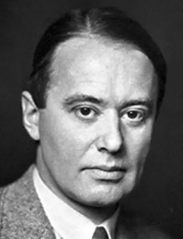
Arne Wilhelm Kaurin Tiselius
抗体结构的解析离不开美国生物学家Gerald Maurice Edelman,他受到Sanger解析胰岛素结构的启发,用B-巯基乙醇处理免疫球蛋白G,分解成两条链,根据分子量大小分别称为重链和轻链,并在此基础上提出了自己心目中的抗体结构:重链和轻链折叠形成奇特的袋状结构,从而识别抗原。

Gerald Maurice Edelman
1963年,Edelman与RodneyRobert Porter(Sanger的第一个博士研究生)结合两人多年的研究结果,提出了比较成熟的抗体分子模型。他们认为,抗体是由两条重链和两条轻链组成的“Y”型对称结构,一条轻链和一条重链的一半组成了“Y”型结构的分支。抗体识别抗原的特异性结合位点位于“Y”型结构的两个分支的顶端,轻链和重链都有一部分包含其中。
1969年,Edelman和Porter完成了一项在当时了不起的成就,他们成功对抗体1300多个氨基酸序列进行了测定,是当时测定氨基酸序列的最大的蛋白质分子。随后Edelman继续深入研究抗体的结构,陆续提出了越来越精确的抗体分子结构,包括重链可变区、重链恒定区、轻链可变区、轻链恒定区以及抗体内部二硫键的位置,同时他认为抗体的差异是由可变区的差异决定的。
通过对抗体结构的不懈研究,抗体识别抗原的结构基础得到了有效阐释,却仍无法回避抗体多样性的基本问题。抗体的分子序列并不固定,免疫系统能够产生不同抗体结合不同的抗原物质。若依据“一个基因编码一条多肽链”的理论,即使人类基因组都无法满足抗体多样性编码的需求。对于这个问题,Edelman和另一位同行Joseph Gaily于1967年提出了一个抗体多样性产生的最初的设想。他们认为编码抗体的基因存在染色体重排现象,识别抗原之后数量有限的抗体基因通过不同的组合形式编码无限种类的抗体分子。
在Edelman提出的抗体多样性理论的基础上,1976年,日本科学家利根川进和同事在检测不产生抗体的胚胎细胞和产生抗体骨髓瘤细胞中抗体轻链基因的分布时发现,胚胎细胞中不同抗体基因距离较远,而骨髓瘤细胞中抗体基因距离接近,这个发现说明生殖细胞在发育成免疫细胞的过程中,抗体基因发生了重新分布现象。利根川进在此基础上用一系列确凿的实验数据确定了抗体多样性是由B淋巴细胞中抗体基冈的染色体重排和突变造成的。根据估算,抗体基因通过重组和突变甚至可以编码100亿种不同的抗体,很好解释了抗体多样性产生的原因。1987年,利根川进由于抗体多样性的突破性研究独享了该年度的诺贝尔生理学或医学奖。

利根川进
-05-
四、治疗性抗体的蓬勃发展
自1986年第一个治疗性抗体进入临床以来,治疗性抗体得到了迅速的发展,其已成为现代生物医药的重要组成部分。到目前为止,全球已获批的抗体药物多达196种, 这些抗体都至少获得一个监管机构的批准。伴随现代科技的发展,治疗性抗体经历了鼠源性抗体,嵌合抗体,改性抗体和表面重塑抗体(部分人源化抗体),以及全人源化抗体等不同发展阶段。
第一代:鼠源单抗(momab)
第一个单克隆抗体药Orthoclone OKT3来自于小鼠,它的氨基酸序列都是鼠源的。鼠源抗体在给病人服用过程中常常遇到一些问题:1)人体把这些单抗药当作异体蛋白,会产生免疫排斥。2)免疫排斥使单抗药很快从病人体内被清除掉,大大降低了它们应有的疗效。尤其治疗慢性疾病需要长期服用的情况下,鼠源单抗药在后续注射时疗效甚微;3)少数病例中,鼠源抗体会引起严重的过敏反应,甚至导致了个别病人的死亡。因此,早期单抗药的销售始终没有腾飞——Orthoclone OKT3的年销售额仅有1千万美元左右。因此,要想在医学上有更广泛的应用,鼠源抗体必须要转变成人源化抗体或人源抗体。
第二代:人鼠嵌合单抗(ximab)和人源化单抗(zumab)
人源化抗体一般是以鼠源抗体为基础,通过更换蛋白片断和置换部分氨基酸序列, 使抗体的最终氨基酸序列更接近人源的,其最终目的是既不引起人的免疫排斥,又不降低它对靶抗原的亲和性。
抗体人源化又分为两个层次。第一个层次是嵌合抗体(Chimeric antibody): 抗体的恒定区都被置换成人的氨基酸序列。嵌合单抗蛋白约33%的氨基酸序列来自小鼠,其余67%为人源的。第二个层次是人源化抗体(Humanized antibody),即拿到针对某抗原的小鼠抗体后,只取其识别抗原的几段区域(CDR区域),把它们移植到人源抗体中。人源化单抗中人源的序列占90%。人源化单抗显然比嵌合单抗更有优势,引起免疫排斥或超敏的风险更低。但即使这样,由于鼠源序列的存在,人源化单抗还是不能完全避免免疫排斥或超敏的风险。
第三代:全人源化单抗(mumab)
获得全人源单抗主要有两种途径:噬菌体展示和转基因小鼠。
噬菌体展示和转基因小鼠在执行过程中各有千秋。一般来说,噬菌体展示技术“先快后慢”,即找到针对某种靶蛋白的抗体很快,但选出的这个抗体和靶蛋白的亲和性往往不高,需要人工细调,更换个别氨基酸。优化这一步费时费力,而且即使优化的抗体和通过转基因小鼠出来的抗体相比,亲和力可能还是相差一个数量级。另外,在优化的过程中需要替换一些氨基酸,也就引进了被免疫排斥的风险。
转基因小鼠技术是“先慢后快”,将抗原注射到小鼠体内、产生特异抗体、制备杂交瘤细胞等前几步需要几个月的时间。但一旦最初的抗体产生,其优化过程在小鼠体内继续完成,又快又好,并且不用担心免疫排斥的问题。
-06-
五、抗体的筛选技术
近年来,随着抗体药的需求越来越大,抗体筛选技术的发展也是日新月异,目前应用较普遍的有杂交瘤技术、抗体文库筛选技术、B细胞克隆技术和转基因小鼠抗体筛选技术。
杂交瘤技术
杂交瘤技术又称为单克隆抗体技术,是在体细胞融合的技术基础上发展而来的。这项技术将免疫动物的B淋巴细胞与骨髓瘤细胞融合,即可形成在体外长期存活并分泌免疫蛋白的杂交瘤细胞,通过克隆化可得到来自单个杂交瘤细胞的单克隆系,即杂交瘤细胞系,利用杂交瘤细胞可以大量的生产单克隆抗体。
细胞融合技术是杂交瘤技术的基础,通过聚乙二醇(PEG)(最常用)、仙台病毒、电转等方法对细胞进行人工诱导,可使两个细胞通过膜融合形成单个细胞。融合细胞的筛选 HAT培养基筛选技术是杂交瘤技术中另一个关键的技术,在B淋巴细胞与骨髓瘤细胞融合后,会产生多种融合结果(未融合的骨髓瘤细胞、未融合的B淋巴细胞、B淋巴细胞自身融合细胞、骨髓瘤细胞自身融合细胞、正确融合的杂交瘤细胞),为了得到所需的杂交瘤细胞,必须利用 HAT 培养基对融合后的细胞进行筛选。
HAT培养基的筛选原理为:DNA合成途径有生物合成途径与应急合成途径两种,HAT培养基中含有次黄嘌呤(H)、氨基喋呤(A)和胸腺嘧啶核苷酸(T)等物质,氨基喋呤可以对 DNA的生物合成途径进行阻断,骨髓瘤细胞会因为生物合成途径被阻断且自身缺乏应急合成途径导致不能增殖进而快速的死亡;而B淋巴细胞因缺乏体外增殖的能力,一般在10天左右死亡;杂交瘤细胞具有体外增殖能力且由于次黄嘌呤与胸腺嘧啶核苷酸的存在,可以通过应急途径合成DNA并在 HAT培养基中正常生长,不会死亡。因此将融合后的细胞放于 HAT 培养基中培养,其他的融合结果会全部死亡,最终筛选出杂交瘤细胞。
噬菌体展示技术
1985年Smith GP利用基因工程,将外源基因插入丝状噬菌体(Filamentous bacteriophage,fd)的基因组,使目的基因编码的多肽以融合蛋白的形式展示,从而创建了噬菌体展示技术。
噬菌体展示技术(phage display)是将外源编码多肽或蛋白质的基因通过基因工程技术插入到噬菌体外壳蛋白结构基因的适当位置,在阅读框能正确表达,使外源多肽或蛋白在噬菌体的衣壳蛋白上形成融合蛋白,随子代噬菌体的重新组装呈现在噬菌体表面,可以保持相对的空间结构和生物活性。然后利用靶分子,采用合适的淘洗方法,洗去未特异性结合的噬菌体。再用酸碱或者竞争的分子洗脱下结合的噬菌体,中和后的噬菌体感染大肠杆菌扩增,经过3-5轮的富集,逐步提高可以特异性识别靶分子的噬菌体比例,最终获得识别靶分子的多肽或者蛋白。除了噬菌体展示技术之外,基于文库展示的技术还包括:酵母展示技术、核糖体展示技术以及细胞展示技术等。
B细胞克隆技术
人和动物接受了外源性免疫原(如细菌、病毒、非同源蛋白等)的刺激后,获得性免疫(Adaptive Immunity)被激活,并在 T 淋巴细胞、巨噬细胞和树突状细胞等免疫细胞的协同作用下,由 B 淋巴细胞产生针对于该病原体(或免疫原)的抗体分子;B 淋巴细胞经过一系列的成熟和分化之后,最终形成浆细胞(Plasma cell)将大量的 IgG 分泌到血液等循环系统中;而特定的某一个 B 淋巴细胞在经历了 V-D-J 重排、Class Switch 和 Somatic maturation 之后,只含有一对编码 IgG 重链和轻链的基因。
因此,经过 B 淋巴细胞表面标记物和抗原特异性筛选,可以获得针对特异性抗原的单个 B 淋巴细胞,然后通过分子生物学手段从中获得编码抗体 IgG 的重链和轻链基因,并在体外重组表达验证,是目前获得单克隆抗体最有效和快速的技术。
基于单 B 细胞筛选的抗体发现技术发展,还得益于流式细胞技术、微流控技术(Microfluidic)以及光流体技术(Optofluidic)等相关生物技术的发展和成熟,使其成功的从实验室走向商业化应用,并在单克隆抗体特别是治疗性单克隆抗体的开发方面被广泛应用。
基于单 B 细胞分选技术的单克隆抗体开发平台,和传统的单克隆抗体开发平台相比,最突出的优势在于能够从人体内直接筛选获得全人源单克隆抗体;同时,也能够大大缩短研发周期,从获得康复病人的外周血淋巴细胞开始,一般来说在 4-6 周内即可获得全人源单克隆抗体,并完成相应的生物学功能实验(如病毒结合和中和实验、ADCC 实验等);并且由于所获得是全人源单克隆抗体,可以大大简化甚至于不需要抗体人源化改造工程,快速推进至临床试验。
转基因小鼠全人源抗体筛选技术
早在1985年,Alt等人就曾提出可以应用转基因技术得到具有人源序列的单克隆抗体。1989年,Bruggemann等人在小鼠中表达了人源重链,从而产生了转基因编码的免疫应答。而在1994年,Lonberg和Jakobovits的团队分别采用了不同的方法构建了能够表达人源抗体的转基因小鼠。Lonberg利用了核内显微注射的方法,而Jakovovits用的是酵母人工染色体(YAC)的方法。重链包含3个重链可变区(VH),16个D,所有的6个JH区。
Abgenix的XenoMouse®是第一个同时有大部分人源VH和人源Vκ repertoire的转基因小鼠品系。这些XenoMouse®小鼠有百万碱基对大小的酵母人工染色体,在重链基因座,有34个有功能的VH基因,全部的DH和JH区域,作为Cμ和Cδ功能下游的人源Cγ2基因;κ轻链基因座含有18个Vκ基因,全部五个功能性的Jκ区,和Cκ基因。由于YAC可以整合到小鼠染色体中,这样得到的小鼠具有较好的基因稳定性。2005年,安进以22亿美元收购Abgenix。XenoMouse平台上开发出的第一个单抗药物是Abgenix和安进共同开发的抗EGFR单抗panitumumab(于2006.9被FDA批准),这也是基于转基因小鼠的第一个全人源单抗药物。
另一个用于产生全人源抗体的小鼠是GenPharm International, Inc开发的HuMab™或者叫Ultimab®。1997年,Medarex收购了该公司获得这一技术平台。2009年,BMS以24亿美元收购Medarex,将Humab小鼠收入囊中。这一平台可产生高亲和力(纳摩到亚纳摩级别)的人源抗体。Ofatumumab是基于Ultimab平台开发出的抗CD20单抗,它和同为CD20抗体的rituximab靶向的表位不同。Ofatumumab于2009年十月被FDA批准用于治疗慢性淋巴细胞白血病。Ultimab平台还有一系列诸如Canakinumab(抗interleukin-1β的IgG1单抗,用于治疗一种罕见的自身炎症性疾病Cryopyrin蛋白相关周期性综合征), Ustekinumab(靶向IL-12和IL-23所共有的p40亚单位,用于18岁及以上活动性银屑病关节炎患者的治疗)等单抗产生。
-07-
结语
抗体药物从发现到进入临床应用,经历了曲折而又漫长的历程。在这段时间里,人们对于抗体药物的认识发生了巨大的变化。在过去的数十年里,抗体已经成为医药市场上最畅销的药物。随着抗体类药物被批准用于治疗各种包括癌症、自身免疫、代谢和传染病,治疗性抗体药物的市场必会呈现爆炸式增长的态势。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#抗体药物# #治疗性抗体#
16 举报