Nature Cancer:推断无法获得的癌前病变的早期遗传进展
2023-05-08 Jenny Ou MedSci原创 发表于上海
本报告为研究前恶性组织无法获得的癌症类型的遗传进展提供了一个框架,该框架能够揭示癌症类型中癌症起始和早期发展的机制,这些癌症的稀有性、难以接近性或缺乏先前性组织使其遗传进展不可破译。

在整个癌症研究历程中,破译遗传病变的时间顺序长期以来一直是癌症研究的目标。该顺序可以为肿瘤发生中的病因学和细胞内在机制提供线索,为正常组织如何成为肿瘤的研究提供信息,还可以提供检测和治疗早期疾病阶段的方法,并将早期克隆事件确定为后期侵袭性肿瘤治疗的有希望靶点。
对于从正常组织有明确病理进展的癌症,沿该轨迹的病变分析提供了相应的遗传进展模型。然而,有许多癌症类型具有定义不清、检测不到或难以进行活检的恶性前期病变,其遗传进展因此仍然是推测性的。
2023年4月20日发表在Nature Cancer上的文章,演示了如何从癌症开始后很久采集的原发性肿瘤样本的外显子组测序中推断出癌症类型遗传事件的典型顺序。研究人员开发了PhylogicNDT,这是一套集成工具,使用连贯的概率框架重建克隆架构和遗传事件的相对时间,并应用PhylogicNDT证明了人类乳头瘤病毒(HPV)阴性头颈部鳞状细胞癌(HNSCC)的遗传进展,并根据结果评估了缺乏前恶性组织的HPV+ HNSCC,并发现了其以前未知的进展,确定了早期驱动因素。
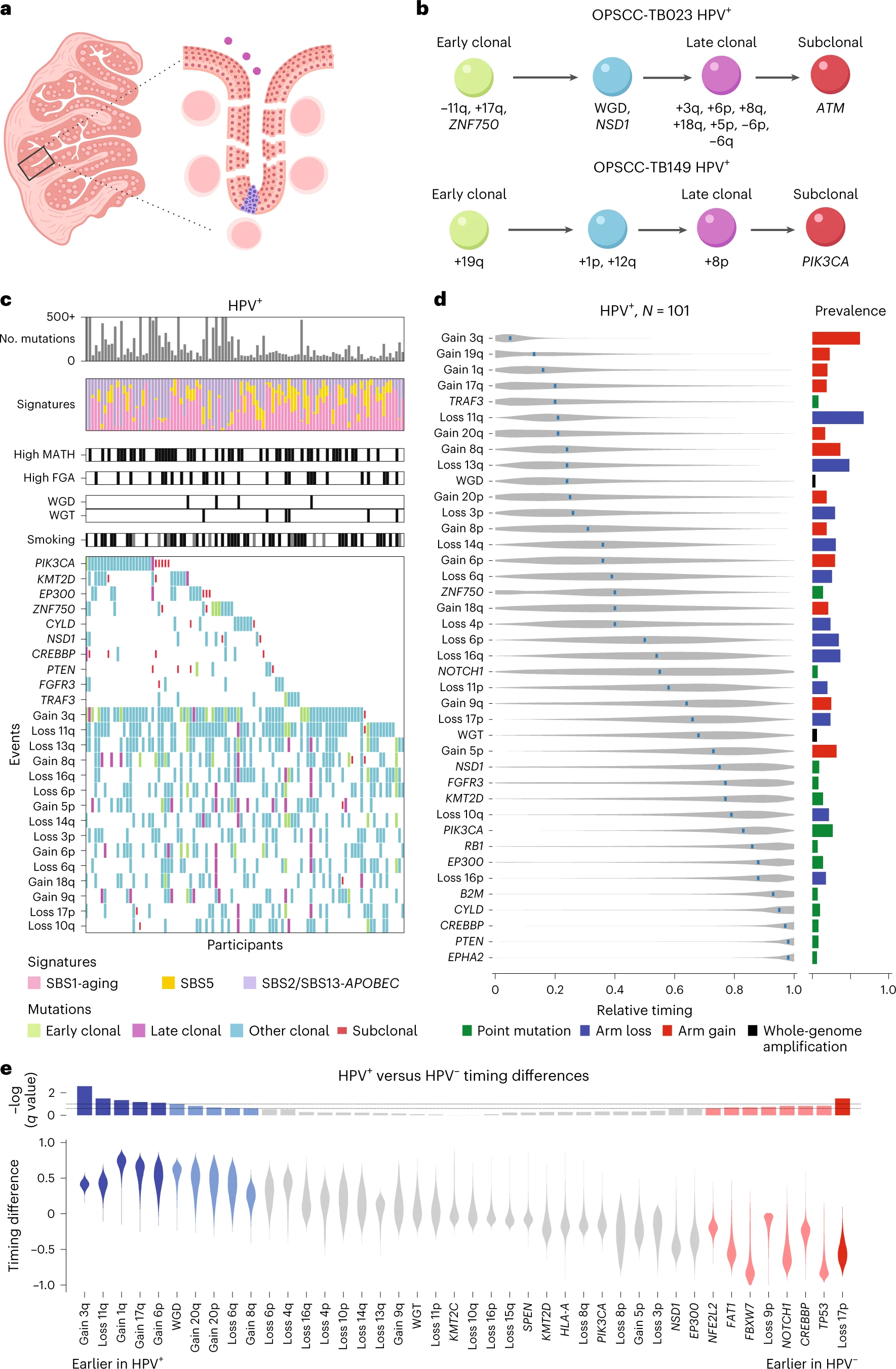
HPV+ HNSCC中的遗传事件及其时间
将HPV- HNSCC的遗传进展模型扩展到总共61个SNV或拷贝数改变事件,其中17个患病率>40%,比较与Califano等人报告的进展阶段相关的事件的预测mRT值,确定了在HPV-肿瘤发生期间导致WGD或WGT的全基因组事件何时发生,在侵袭性癌症的临床发展之前或附近得出了估计值。
研究人员确定了早期突变的基因(FBXW7、NOTCH1、CASP8、FAT1、NSD1、HRAS、EP300、CREBBP和KMT2D),这些基因可能在HPV-肿瘤启动中发挥作用,超过60%的HPV- HNSCC至少在其中一个基因中具有突变。其中,CASP8突变几乎仅在口腔中,NSD1在喉部肿瘤中占主导地位。相比之下,长期怀疑在HPV- HNSCC中发挥作用的NOTCH1突变肿瘤与其他HPV- HNSCC没有解剖偏好或频率或时间差异。后期mRT(PK3CA、NFE2L2、HLA-A、SPEN和KMT2C)有突变的基因对进展到疾病的后期阶段更有可能很重要。
在HPV+ HNSCC中,染色体臂3q的增加和臂11q的损失都比HPV-HNSCC更早、更频繁,这表明在HPV+进展中起着重要的早期作用。Arm 3q包括PIK3CA位点,其通过拷贝数增益或突变的激活经常发生在HNSCC中;74%的HPV+和62%的HPV-HNSCC表现出与PIK3CA位点相关的遗传改变。在HPV+肿瘤的mRT中发现3q的增益比在HPV-肿瘤中,这表明PIK3CA在HPV+疾病中扩增具有特别重要的早期作用。
关于HPV+ HNSCC损失11q,ATM是早期参与肿瘤形成的候选者。虽然ATM提高了表观染色体HPV的复制能力,但它在防止双链DNA断裂方面的作用,预计将抑制HPV DNA的基因组整合。11q的损失也发生在HPV-疾病中,但更晚的mRT为0.67,估计十分接近原位癌的发展。
使用类似时钟的突变特征将相对事件时间估计值转换为诊断前的几年,研究人员确定早期创始事件可以在HPV-疾病肿瘤诊断前30-40年发生,在HPV+肿瘤中可能发生20-30年或更长时间,HPV整合也在开发早期。WGD到WGT的转换似乎遵循一个突然的过渡模型,每年有特定的过渡概率。
这项工作有助于澄清与结果相关的基因组破坏措施的性质。几乎所有导致WGT或WGD的全基因组事件的肿瘤都有很高的数学值。当考虑治疗和标准临床和病理特征时,高FGA也与HNSCC的总体生存期较短有关。基因组破坏的测量可用于将个体分为高风险和低风险组,以使用最小残留疾病检测等策略来监测疾病。入侵前确定WGD时间可用于识别HPV-HNSCC的进展风险更高。其他早期驱动因素可能是额外治疗试验的基础,包括在高风险个体的预防环境中。
将本文的方法应用于癌症前恶性组织很少或永远无法获得的癌症,具有重要的临床意义。由于许多此类癌症的病因不确定,与更普遍的肿瘤相比,有效的治疗途径不那么明确。建立进展轨迹、早期驱动因素和进展与其他癌症类型的相似性可以导致开发更好的疾病模型、更好的治疗策略和临床管理,以及更准确地预测疾病过程。
原文出处
Leshchiner, I., Mroz, E.A., Cha, J. et al. Inferring early genetic progression in cancers with unobtainable premalignant disease. Nat Cancer 4, 550–563 (2023). https://doi-org.7sup.top/10.1038/s43018-023-00533-y
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言