Brain:表征阿尔茨海默病中淀粉样蛋白时间线的脑 tau 和认知能力下降
2024-09-25 MedSci原创 MedSci原创 发表于上海
淀粉样蛋白时间框架能够对阿尔茨海默病连续体中的tau沉积模式进行时空表征。
最近的纵向 PET 成像研究已经建立了估计淀粉样蛋白在个体水平上变得异常的年龄的方法。在这里,我们将淀粉样蛋白水平重新置于时间域中,以更好地了解下游阿尔茨海默病的 tau 神经原纤维缠结 (NFT) 积累和认知能力下降的过程。

该队列研究包括来自威斯康星州阿尔茨海默病预防登记处和威斯康星州阿尔茨海默病研究中心的 601 名个体,他们接受了淀粉样蛋白和 tau PET、纵向神经心理学评估并符合三个临床诊断组的临床标准:认知无障碍 (n = 537);轻度认知障碍 (n = 48);或痴呆 (n = 16)。皮质 11C-匹兹堡化合物 B (PiB) 分布体积比 (DVR) 和采样迭代局部近似用于估计淀粉样蛋白阳性 (A+;整体 PiB DVR > 1.16 相当于 17.1 厘)在 tau PET 的发病年龄和 A+ 持续时间的年份 (即 淀粉样蛋白慢性)。使用 18个 F-MK-6240 标准化摄取值比 (70-90 min,小脑下灰质参考区) 量化 Tau PET 负荷。全脑和区域特异性方法用于检查沿淀粉样蛋白时间线和阿尔茨海默病临床连续体的 tau PET 结合。
体素 18F-MK-6240 分析显示,在 A+ 的每个十年中,可测量的 tau 传播的空间范围(即 进展)从早期到晚期 NFT tau 阶段相关的区域。区域分析表明,平均在 A+ 发作后 10 年内可检测到内嗅皮层中的 tau 负荷。此外,在这个主要是临床前样本中,内嗅皮层是对早期淀粉样蛋白病理和临床损伤最敏感的区域。在最初认知未受损 (n = 472) 的纵向认知随访个体中,混合效应模型显示 A+ 持续时间和内嗅 tau 对认知能力下降的显着线性和非线性相互作用,表明协同效应,即更长的 A+ 持续时间,以及更高的内嗅 tau 负担,增加了认知能力下降的可能性超出其可分离的影响。
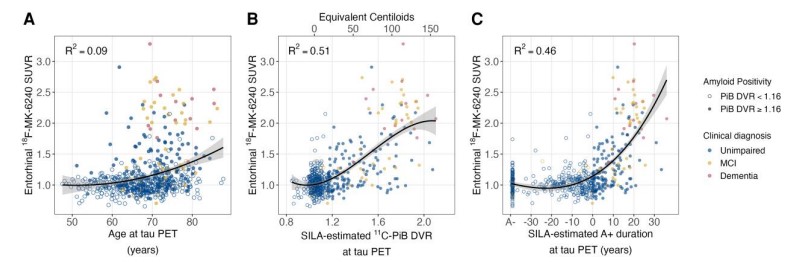
总体而言,淀粉样蛋白时间框架能够对阿尔茨海默病连续体中的tau沉积模式进行时空表征。这种方法检查了沿淀粉样蛋白时间线的横断面 tau PET 数据,以做出纵向病程推断,表明 A+ 持续时间解释了 tau 传播的幅度和地形的大量可变性,这在很大程度上概括了在人类神经病理学研究中观察到的 NFT 分期。通过将疾病进展锚定在淀粉样蛋白的发病上,这项研究提供了一个时间疾病背景,这可能有助于为疾病预后和抗淀粉样蛋白治疗的时间窗口提供信息。
原始出处:
Characterizing brain tau and cognitive decline along the amyloid timeline in Alzheimer’s disease, Brain, Volume 147, Issue 6, June 2024, Pages 2144–2157, https://doi.org/10.1093/brain/awae116
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






















#阿尔茨海默病# #淀粉样蛋白#
76
新的进展产生新的治疗!!!!
65