CHC:找到心肌细胞停滞发育的元凶!曾春雨教授:LncRNA-DRR通过竞争性结合SFPQ蛋白,抑制DNA的修复,引起心肌细胞周期停滞
2022-09-22 网络 网络
心肌梗死是一种全球范围内发病率较高的危重心血管疾病,随着急诊冠脉介入等临床诊疗水平的提高,90%以上的心梗患者均能存活。但仍有25%患者再出院后1年内出现心力衰竭,大幅度增加了死亡风险。
心肌梗死是一种全球范围内发病率较高的危重心血管疾病,随着急诊冠脉介入等临床诊疗水平的提高,90%以上的心梗患者均能存活。但仍有25%患者再出院后1年内出现心力衰竭,大幅度增加了死亡风险。
心肌梗死发生后,高达1/4心肌细胞发生死亡,而既往一致认为“心肌细胞不可再生”,成纤维细胞便将替代损伤的心肌细胞,导致心功能下降,逐渐发展成心力衰竭。
近些年,“心肌细胞不具备自我修复能力”的观念被打破,有学者指出“成年心肌以极低速率进行自我更新,虽然效率十分有限”。
此“再生能力”来源于原有心肌细胞的增殖分裂,而非外界传言的“心肌干细胞”。
很明显想要逆转心衰,必须改变内源性心肌细胞修复“慢悠悠地”效率。这成为当前研究的重点问题。
研究显示,心肌细胞增殖能力自出生后迅速下降,28天时基本消失,因此出生内外环境的变化成为大家关注的焦点。
研究者首先成功建立新生小鼠(出生第一天)心间切除模型,通过高通量测序,发现LncRNA-DRR在心尖切除术后显著下调。
为了反复验证LncRNA-DRR对心脏发育的影响,研究者又造了LncRNA-DRR敲除小鼠模型,结果发现,该模型小鼠心脏结构、大小及心肌细胞增殖无显著变化,即它不影响心脏本身的发育。同时,LncRNA-DRR敲除小鼠心肌细胞增殖能力发生明显改变(上升),心肌梗死后肺纤维化水平显著下降。
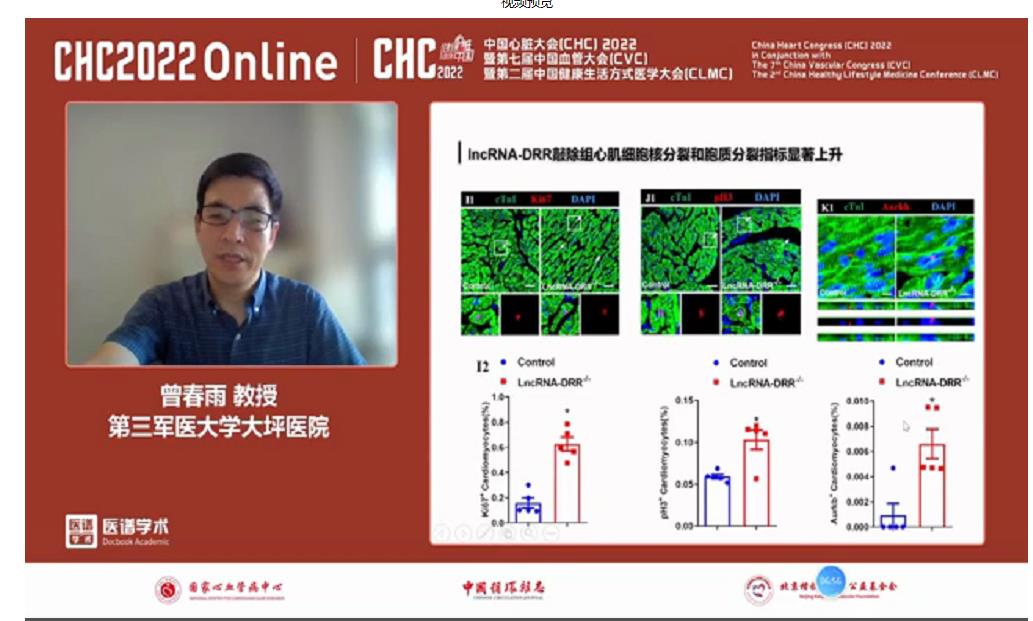
发生这一变化可能的机制是细胞周期和DNA损伤后修复信号通路发生显著变化。

随后研究者又通过数据库,预测发现LncRNA-DRR与DNA损伤后相关蛋白SFPQ具有结合潜能:LncRNA-DRR通过竞争性结合SFPQ蛋白,影响SFPQ/NONO蛋白复合体的形成,抑制DNA的修复,引起心肌细胞周期停滞。这一机制的发现,为进一步“尝试改变心肌细胞低效增殖速度”的探索者拨开了部分理论迷雾。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言