Cell Res | 红细胞 DNA 残留助力早期癌症精准检测
5小时前 MedSci原创 MedSci原创 发表于上海
本研究通过分析红细胞中的 DNA 残留(rbcDNA),为早期癌症检测提供了一种新的潜在生物标志物。
癌症是全球第二大死亡原因,其发病率和死亡率持续上升。早期检测癌症对于提高患者生存率至关重要,但目前大多数癌症在确诊时已处于晚期,主要原因是缺乏有效的筛查方法。近年来,液体活检技术尤其是基于循环游离DNA(cfDNA)和循环肿瘤DNA(ctDNA)的方法在非侵入性癌症检测中显示出潜力,但由于早期癌症患者中ctDNA含量有限、半衰期短以及受到克隆性造血和非癌组织体细胞突变的干扰,其诊断效果受到限制。因此,寻找更稳定、更强大的早期癌症生物标志物成为当务之急。
近日,国际权威期刊Cell Research上在线发表了题为“DNA remnants in red blood cells enable early detection of cancer”的最新研究成果。该研究分析了健康个体和癌症患者的 rbcDNA,发现早期实体瘤患者的 rbcDNA 具有独特的基因组特征,与健康供体存在显著差异。研究人员开发了一种三步法从外周血中分离和纯化 rbcDNA,并通过原子力显微镜(AFM)成像和全基因组测序(WGS)发现,rbcDNA 主要由短 DNA 片段组成,平均长度约为 4.3 千碱基对(kb),远长于 cfDNA,且在内含子和外显子区域富集,而在基因间区域较少。此外,rbcDNA 中线粒体 DNA(mtDNA)的比例远低于白细胞 DNA。

研究纳入了 236 名健康供体(HDs)和 174 名早期结直肠癌(CRC)患者,发现 CRC 患者的 rbcDNA 在基因组分布上与 HDs 有显著差异,特别是在基因间和着丝粒区域。研究人员识别出 246 个基因组区域,这些区域在 CRC 患者的 rbcDNA 读数计数上与 HDs 存在显著差异,被称为 CRC 相关 rbcDNA 特征。这些特征中,86.18% 与之前识别的 rbcDNA 富集区域不重叠,且多数与静止染色质区域相关,表明形成肿瘤相关 rbcDNA 特征的潜在机制与正常 rbcDNA 富集区域不同。
研究人员利用机器学习模型(XGBoost)对 CRC 相关 rbcDNA 特征进行分析,最终确定了 16 个最优特征,用于区分 HDs 和 CRC 患者。在测试集中,该模型实现了 97% 的曲线下面积(AUC),在 96% 的特异性下,对 CRC 患者的敏感性达到 94%,包括 89% 的 I 期、100% 的 II 期和 91% 的 III 期癌症患者。此外,该模型还能准确区分出患有高级别腺瘤和早期腺瘤的患者。为了进一步验证模型的泛化能力,研究人员在包含多种癌症类型(包括肺癌、胃癌、乳腺癌、甲状腺癌和 CRC)的独立队列中进行了测试,发现该模型在 96% 的特异性下,对各种癌症类型的检测敏感性达到 87%,且能以 72% 的准确率识别肿瘤组织来源。
研究人员利用 Apcmin/+ 小鼠模型(一种易患肠道肿瘤的小鼠模型)来研究肿瘤相关 rbcDNA 特征的形成机制。结果显示,与野生型(WT)小鼠相比,Apcmin/+ 小鼠的 rbcDNA 在基因组分布上存在显著差异,且这些差异与肿瘤进展相关。通过蛋白质组学分析,研究人员发现 IL-18 结合蛋白(IL-18BP)在肿瘤小鼠血清中显著上调,IL-18 是一种与 DNA 损伤和细胞凋亡相关的炎症因子。进一步研究发现,IL-18 在肿瘤小鼠血清中的水平随着肿瘤进展而增加,且在早期 CRC 患者中也观察到 IL-18 水平的升高。通过给 Apcmin/+ 小鼠注射抗 IL-18 抗体,研究人员发现可以显著降低 rbcDNA 特征的读数计数,且不影响肿瘤生长,这表明 IL-18 对于肿瘤相关 rbcDNA 特征的形成至关重要。此外,研究人员还发现 IL-18 信号通路的激活导致骨髓造血细胞中 DNA 损伤的增加,特别是造血干细胞和祖细胞(HSPCs)中 γH2AX(DNA 双链断裂的标志物)和微核的频率显著升高。通过染色质免疫沉淀测序(ChIP-seq)分析,研究人员发现 NR4A1(一种孤儿核受体)在 IL-18 高表达的 HSPCs 中显著富集,并与肿瘤相关 rbcDNA 特征区域重叠。NR4A1 的上调与 DNA 损伤、细胞周期调控和染色体分离途径相关基因的表达增加有关。研究人员还通过体外实验验证了 IL-18 和 NR4A1 在 rbcDNA 特征形成中的作用,发现 IL-18 处理的 HSPCs 中 NR4A1 的结合增加,且 NR4A1 拮抗剂 DIM-C-pPhOH 可以抑制 rbcDNA 特征的形成。
综上所述,本研究通过分析红细胞中的 DNA 残留(rbcDNA),为早期癌症检测提供了一种新的潜在生物标志物。研究发现,早期实体瘤患者的 rbcDNA 具有独特的基因组特征,这些特征与肿瘤进展密切相关,并且可以通过机器学习模型实现高准确度的癌症检测。此外,研究还揭示了白介素 - 18(IL-18)在肿瘤相关 rbcDNA 特征形成中的关键作用,其通过激活 NR4A1 导致骨髓造血细胞中的 DNA 损伤,进而影响 rbcDNA 的特征。这些发现不仅为癌症的早期诊断提供了新的策略,也为理解肿瘤与造血系统之间的相互作用提供了新的见解。
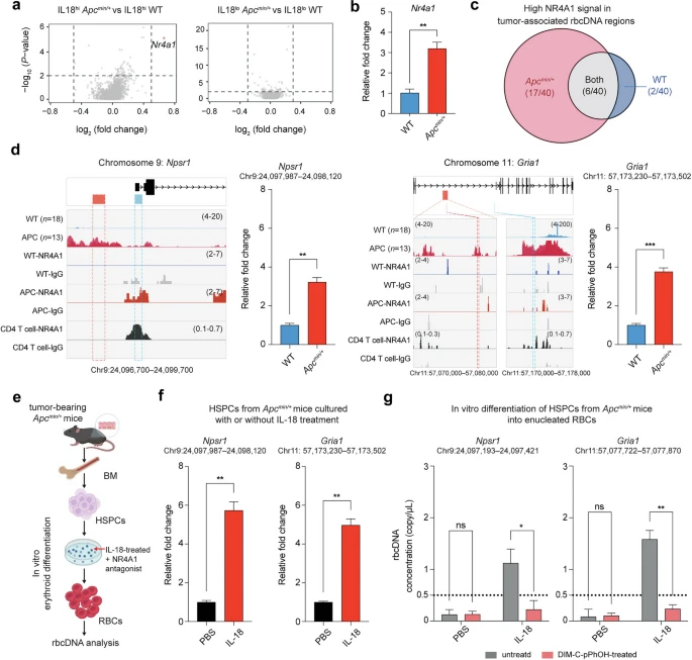
图 NR4A1对于肿瘤相关rbcDNA特征的形成至关重要
原始出处:
DNA remnants in red blood cells enable early detection of cancer. Cell Res. 2025 May 9. doi: 10.1038/s41422-025-01122-7. Epub ahead of print. PMID: 40341742.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















前往app查看评论内容
0 0
前往app查看评论内容
0 0
前往app查看评论内容
0 0
前往app查看评论内容
5 0