南方医科大学Science子刊:来自癌症相关成纤维细胞的细胞外囊泡包装PIAT通过介导m5C修饰驱动神经重塑
2024-07-22 BioMed科技 BioMed科技 发表于上海
研究显示,这些EV与PNI相关转录物(PIAT)包装在一起,在小鼠模型中可增强PNI并诱导更差的存活率。因此,PIAT是减少癌症PNI的潜在靶点,并有望提高患者的生存率。
胰腺癌症的预后通常非常差,这主要以神经周围侵犯(PNI)为特征;然而,PNI在术后生存中的作用尚未得到充分的探索。在此,南方医科大学Rufu Chen、Yu Zhou和中山大学Changhao Chen等人评估了PNI在胰腺癌症预后中的作用,并表明癌症相关成纤维细胞(CAFs)通过CAF衍生的细胞外囊泡(EVs)诱导肿瘤中的PNI。研究显示,这些EV与PNI相关转录物(PIAT)包装在一起,在小鼠模型中可增强PNI并诱导更差的存活率。因此,PIAT是减少癌症PNI的潜在靶点,并有望提高患者的生存率。相关工作以“Extracellular vesicle–packaged PIAT from cancer-associated fibroblasts drives neural remodeling by mediating m5C modification in pancreatic cancer mouse models”为题发表在Science Translational Medicine。

【文章要点】
临床样本分析和内镜超声弹性评分表明,癌症相关成纤维细胞(CAFs)与PNI的发生密切相关。此外,在背根神经节共培养和小鼠坐骨神经模型中,CAF衍生的细胞外囊泡(EV)参与了PNI。因此,在本研究中,证明CAFs通过PNI相关转录物(PIAT)的细胞外囊泡传递促进PNI。从机制上讲,PIAT特异性结合YBX1并阻断YBX1-Nedd41相互作用,从而抑制YBX1泛素化和降解。此外,PIAT以5-甲基胞嘧啶(m5C)依赖的方式增强YBX1和PNI相关mRNA的结合(图1)。
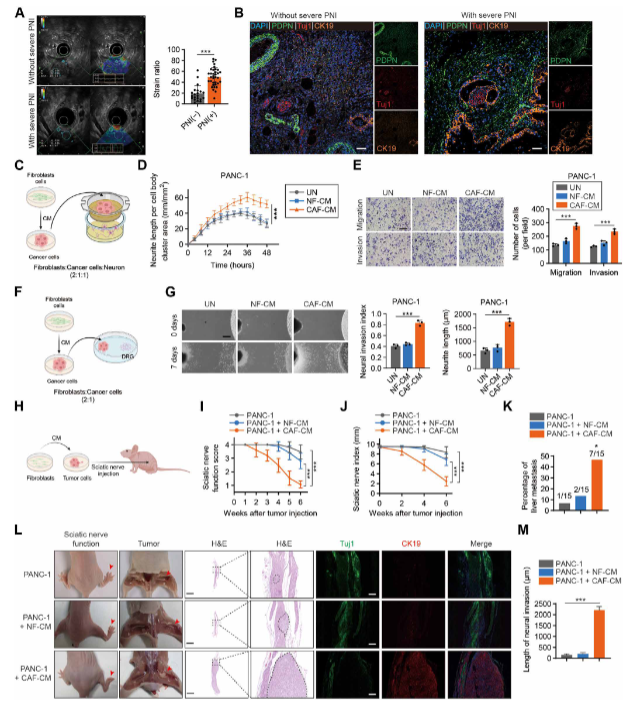
图1 CAFs增强胰腺癌的PNI
下游靶基因YBX1或m5C位点的m5C识别基序突变逆转了PIAT介导的PNI。与这些发现一致,使用KPC小鼠模型的分析表明,PIAT/YBX1轴通过m5C修饰增强了PNI。临床资料表明,癌症患者血清EVs中PIAT的表达与神经侵袭程度和预后有关。该研究揭示了PIAT/YBX1信号轴在肿瘤微环境(TME)中促进肿瘤细胞PNI的重要作用,并为精确干扰TME中的CAFs和RNA甲基化以抑制癌症中的PNI提供了新的靶点(图2)。
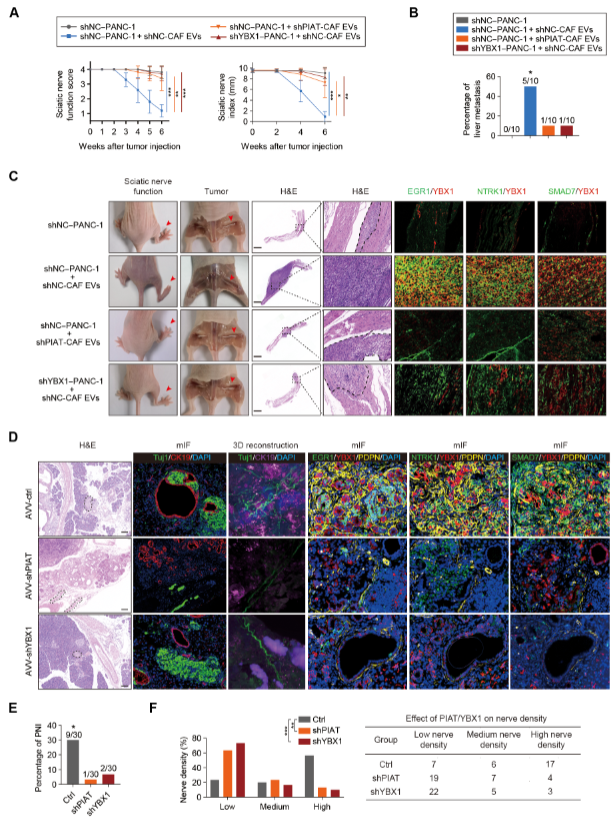
图2 CAFs通过EV释放PIAT以在体内增强胰腺癌的PNI
原文链接:
https://www.science.org/doi/10.1126/scitranslmed.adi0178
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#胰腺癌# #细胞外囊泡# #癌症相关成纤维细胞# #神经周围侵犯#
179