国内EGFR-TKI革新:一览国内三代EGFR抑制剂在非小细胞肺癌治疗中的风云内卷!
2024-01-29 MedSci原创 MedSci原创 发表于上海
根据EGFR-TKI对不同类型的EGFR突变的抑制能力和选择性,可以将其分为一代、二代和三代。
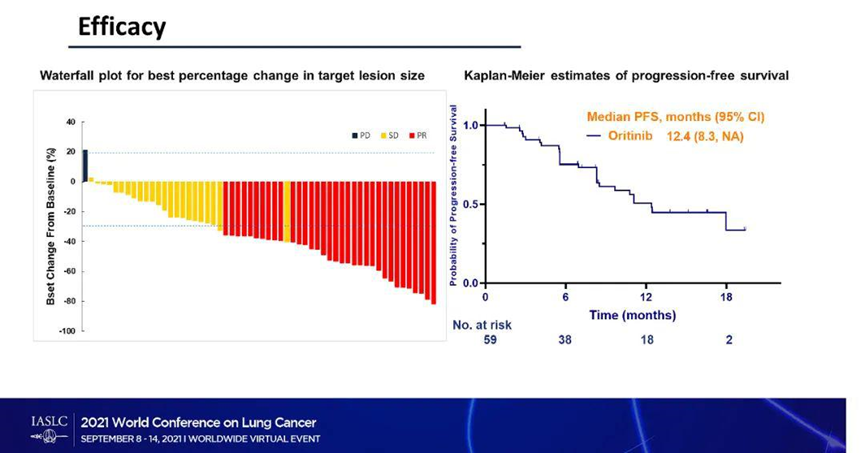
根据EGFR-TKI对不同类型的EGFR突变的抑制能力和选择性,可以将其分为一代、二代和三代。 一代EGFR-TKI主要针对敏感突变(如19外显子缺失或21外显子L858R突变),但不能克服耐药突变(如20外显子T790M突变)。 二代EGFR-TKI可以同时抑制敏感突变和部分耐药突变,但仍不能克服T790M突变,并且对野生型EGFR(即正常细胞中的EGFR)也有较强的抑制作用,导致不良反应增加。 三代EGFR-TKI则可以有效地抑制T790M突变,并且对野生型EGFR有较弱的抑制作用,从而提高了疗效和安全性。 一、第三代EGFR-TKI数据列表 PART/ 01 1. 奥希替尼 奥希替尼是第三代 EGFR-酪氨酸激酶抑制剂 (EGFR-TKI),可有效且选择性地抑制 EGFR-TKI 致敏和EGFR T790M 耐药突变。2019年8月,基于FLAURA研究数据,中国NMPA正式批准奥希替尼一线治疗EGFR敏感突变(19号外显子缺失或L858R突变)的NSCLC。 FLAURA研究是一项国际多中心、随机、对照Ⅲ期临床研究,旨在评估奥希替尼单药(80mg PO QD,n=279)或标准EGFR-TKIs治疗(SoC,包括吉非替尼 250mg PO QD或厄洛替尼 150mg PO QD,n=277)一线治疗EGFR敏感突变阳性晚期NSCLC患者的疗效和安全性。 主要终点PFS首先达到阳性:无进展生存期达到18.9个月,相较对照组10.2个月,延长了8.7个月,HR=0.46,降低了54%的进展或死亡风险! 关键次要研究终点OS实现历史性突破达到阳性终点,在FLAURA研究中,尽管有1/3使用一代TKI的患者耐药后交叉到了奥希替尼组(即对照组中1/3数据是一代/二代耐药后序贯奥希替尼的数据),但是最终的总生存时间,奥希替尼一线使用组仍然达到38.6个月,相比一代TKI组31.8个月的中位OS,延长了6.8个月的生存时间,具有显著统计学意义及临床意义(HR=0.799,P=0.0462)!两组3年生存率为54% vs 44%。 这是EGFR-TKI药物在EGFR阳性人群的首次OS突破!也表明1/2代+3代的序贯模式,在生存获益上并不及一线直接用三代TKI奥希替尼。 2.阿美替尼 阿美替尼是我国首个自主研发的三代表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)。 AENEAS研究是一项评价阿美替尼作为一线治疗方案疗效和安全性的多中心、随机、双盲Ⅲ期研究。试验共纳入429例携带EGFR19外显子缺失或L858R突变的晚期NSCLC患者,1:1随机接受阿美替尼或吉非替尼治疗,治疗直至疾病进展或毒性不可耐受。 研究主要终点为无进展生存期(PFS),次要终点包括总生存(OS),客观缓解率(ORR),反应持续时间(DoR)和安全性。 研究结果显示,使用阿美替尼作为一线治疗的患者,无进展生存期(PFS)及持续缓解时间(DoR)均显著延长——mPFS 19.3个月 vs 9.9个月(HR 0.46 , P<0.0001),mDoR 18.1个月 vs 8.3个月(HR 0.38 , P<0.0001)。 安全性方面,尽管阿美替尼组治疗持续时间更长(中位463天vs 254天),但是皮疹、腹泻、AST/ALT升高和治疗相关严重不良事件(4.2% vs 11.2%)发生率更低。 2022年6月,伏美替尼已在国内获批单药一线治疗EGFR ex19 DEL或ex21 L858R置换突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。 伏美替尼一线治疗 EGFR 突变 NSCLC 的适应症上市申请基于 III 期注册临床 FURLONG 研究,旨在对比伏美替尼和一代 EGFR-TKI 吉非替尼一线治疗 EGFR 突变 NSCLC 的疗效和安全性,研究共纳入 358 名患者。 研究结果显示,伏美替尼一线治疗中国晚期 EGFR 敏感突变晚期非小细胞肺癌患者可带来 20.8 个月的中位无进展生存期(PFS),相比吉非替尼治疗组的 11.1 个月 PFS,延长了 9.7 个月,相较于当前三代 EGFR-TKI 类药物单药一线治疗的最长 PFS 数据也有 1.5 个月的提升;患者疾病进展或死亡风险降低 56%。 同时其入组人群中还有近一半(49%)为 EGFR L858R 突变人群,三分之一伴有脑部转移的人群,这两组人群当前仍属于难治型肺癌,FURLONG 研究结果显示前者的疾病进展或死亡风险降低 46%,后者也有 50% 的降幅,疗效亮眼。 二、众望更多国产三代EGFR-TKI获批上市 PART / 02 2021年12月28日,国家药品监督管理局药品审评中心(CDE)官网显示,第三代EGFR酪氨酸激酶抑制剂(EGFR-TKI)甲磺酸奥瑞替尼片(代号:SH-1028)上市申请获国家药品监督管理局(NMPA)受理。 甲磺酸奥瑞替尼片(SH-1028片)为国产第三代EGFR-TKI,不可逆地结合于突变形式的EGFR(T790M、L858R和19外显子缺失),主要作用在EGFR的激酶结构域,竞争性结合于激酶上的ATP位点,抑制EGFR的磷酸化过程,阻断下游信号通路的激活。临床前的体内外研究均表明奥瑞替尼对野生型EGFR激酶具有较高的选择性。 1.临床数据 此前,在2021年9月召开的2021年世界肺癌大会(WCLC)上以壁报形式公布了一项开放性、多中心Ib期研究,旨在评估奥瑞替尼治疗局部晚期或转移性非小细胞肺癌(NSCLC)患者的疗效和安全性。 在该研究中,共有59例患者接受了奥瑞替尼治疗并纳入全分析集,所有受试者均为肺腺癌,并且经中心实验室检测为EGFR T790M阳性。所有入组患者每天口服给药一次,21天为一个治疗周期,连续给药直至疾病进展或者出现不能耐受的不良反应。 入组患者的人群特征包括:中位年龄为62.0岁;64.4%为女性患者;76.3%患者无吸烟史;ECOG评分为0(15.3%)、1(83.1%)、2(1.7%);35.6%的患者基线时存在脑转移;既往中位治疗线数为1(范围0~3),其中47.5%的患者既往接受过化疗。 试验结果显示,在59例EGFR T790M突变阳性的受试者中,由独立中心审查委员会(BICR)评估的客观缓解率(ORR)为57.6%,部分缓解(PR)为57.6%;疾病控制率(DCR)为98.3%;中位无进展生存期(PFS)为12.4个月;中位持续缓解时间(DOR)为15.2个月;中位总生存期(OS)尚未达到。 由研究者评估的ORR为54.2%,完全缓解(CR)为1.7%,PR为52.5%;DCR为96.6%;中位PFS为11.7个月;中位DOR为11.1个月;中位OS尚未达到。 此外,研究结果表明200mg剂量水平的奥瑞替尼对EGFR T790M突变阳性的NSCLC患者有良好的治疗效果,并可显著延长NSCLC患者的疾病进展时间。 此外,研究结果表明200mg剂量水平的奥瑞替尼对EGFR T790M突变阳性的NSCLC患者有良好的治疗效果,并可显著延长NSCLC患者的疾病进展时间。 安全性及结论
3.伏美替尼

PART/ 03
安全性
在安全性方面,在所有与奥瑞替尼相关的不良反应(TRAE)中,大多数为轻度或中度,仅有10例(16.9%)患者发生≥3级的TRAE,2例(3.4%)患者发生严重的TRAE。
奥瑞替尼常见的不良反应(≥10%)包括:腹泻(52.5%)、血肌酸磷酸激酶升高(37.3%)、血小板计数降低(13.6%)、天门冬氨酸氨基转移酶升高(13.6%)、白细胞计数降低(13.6%)、α-羟丁酸脱氢酶升高(13.6%)、丙氨酸氨基转移酶升高(10.2%)、血肌酐升高(10.2%)、血乳酸脱氢酶升高(10.2%)等。
结论
奥瑞替尼的Ib期临床研究数据为其用于EGFR T790M突变阳性的NSCLC患者的治疗提供了有力支持,也为NSCLC患者提供了更优的治疗选择。期待能早日上市,造福患者!
截止目前,国内已有3款第3代EGFR-TKI上市,此前,阿斯利康的奥希替尼于2017年3月22日获NMPA批准上市。目前已获批用于NSCLC一线、二线以及术后辅助治疗。
豪森阿美替尼是在国内获批上市的首款国产3代EGFR-TKI,目前已获NMPA批准用于NSCLC一线、二线治疗。
艾力斯医药的伏美替尼是国内第3款获批上市的EGFR-TKI,于今年3月获批上市,用于NSCLC二线治疗,其一线适应症也已于近日递交了上市申请并被纳入了优先审评。
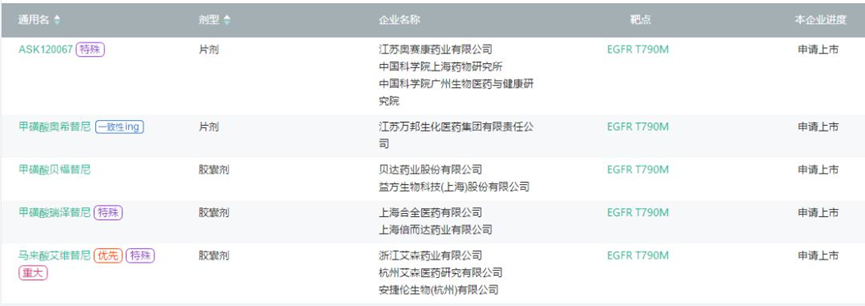
此外,国内还有贝达药业(贝福替尼)、合全医药(瑞泽替尼)、艾森医药(艾维替尼)、奥赛康(ASK120067)申报各自3代EGFR-TKI新药上市,目前处于“上市审评”阶段。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






